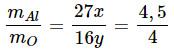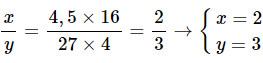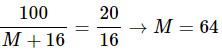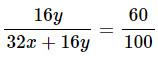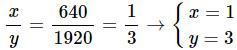Tóm tắt và giải hóa lớp 8 bài 25: Sự oxi hóa – Phản ứng hóa hợp – Ứng dụng của oxi
Tóm tắt và giải hóa lớp 8 bài 25: Sự oxi hóa – Phản ứng hóa hợp – Ứng dụng của oxi
Mục lục
Dưới đây là bài tóm tắt và giải hóa lớp 8 bài 25 mà bạn có thể tham khảo để học hóa tốt hơn !
1. Tóm tắt hóa học lớp 8 bài 25:
– Sự tác dụng của oxi với một chất là sự oxi hóa.
– Phản ứng hóa hợp là phản ứng hóa học trong đó có một chất mới (sản phẩm) được tạo thành từ hai hay nhiều chất ban đầu.
– Ứng dụng: Khí oxi cần cho sự hô hấp của con người và động vật, cần để đốt nhiên liệu trong đời sống và sản xuất.
2. Hướng dẫn giải bài tập Hóa học 8 bài 25:
Bài 1 trang 87
Dùng cụm từ thích hợp trong khung để điền vào chỗ trống trong các câu sau :
| một chất mới | sự oxi hóa | đốt nhiên liệu | sự hô hấp | chất ban đầu |
a) Sự tác dụng của oxi với một chất là …………………
b) Phản ứng hóa hợp là phản ứng hóa học trong đó chỉ có……………………..được tạo thành từ hai hay nhiều ………………
c) Khí oxi cần cho ………………… của người và động vật và cần để ………………….trong đời sống và sản xuất.
Bài giải:
a) Sự tác dụng của oxi với một chất là sự oxi hóa.
b) Phản ứng hóa hợp là phản ứng hóa học trong đó chỉ có một chất mới được tạo thành từ một hay nhiều chất ban đầu.
c) Khí oxi cần cho sự hô hấp của người và động vật cần để đốt nhiên liệu trong đời sống và sản xuất.
Bài 2 trang 87
Lập phương trình phản ứng hóa học biểu diễn phản ứng hóa hợp của lưu huỳnh với các kim loại magie Mg, kẽm Zn, sắt Fe, nhôm Al, biết rằng công thức hóa học của các hợp chất được tạo thành là MgS, ZnS, FeS, Al2S3.
Bài giải:
Phương trình hóa học:
Mg + S MgS
Fe + S FeS
Zn + S ZnS
2Al + 3S Al2S3
Bài 3 trang 87
Tính thể tích oxi cần thiết để đốt cháy hoàn toàn lượng khí metan CH4 có trong 1 m3 khí chứa 2% tạp chất không cháy. Các thể tích đo ở đktc.
Bài giải:
Ta có: 1 m3 = 1000 dm3 = 1000 lít
Phần trăm của metan là: % CH4 = 100% – 2% = 98%
Lượng khí CH4 nguyên chất là:
VCH4 = (1000 x %CH4) / 100% = (1000 x 98%) / 100% = 980 (lít)
Số mol khí CH4 là:
nCH4 = VCH4 / 22,4 = 980/22,4 = 43,75 (mol)
Phương trình hóa học:
CH4 + 2O2 CO2 + 2H2O
PT: 1 mol → 2 mol
ĐB: 43,75 mol → ? mol
Số mol O2 là:
nO2 = 2nCH4 = 2 x 43,75 = 87,5 (mol)
Thể tích khí O2 là:
VO2 = nO2 x 22,4 = 87,5 x 22,4= 1960 (lít)
Bài 4 trang 87
a) Hãy dự đoán hiện tượng xảy ra và giải thích hiện tượng đó khi cho một cây nến đang cháy vào một lọ thủy tinh rồi đậy nút kín.
b) Vì sao khi tắt đèn cồn người ta đậy nắp đèn lại ?
Bài giải:
a) Khi cho cây nến đang cháy vào một lọ thủy tinh và đậy nắp kín, ngọn lửa cây nến sẽ yếu dần rồi tắt, đó là vì khi nến cháy lượng oxi trong lọ sẽ bị giảm dần rồi hết, lúc đó nến sẽ bị tắt.
b) Khi tắt đèn cồn người ta đậy nắp đèn lại vì để ngăn không khí tiếp xúc với ngọn lửa đèn cồn nghĩa là không có oxi tiếp xúc cồn không cháy được nữa.
Bài 5 trang 87
Hãy giải thích vì sao :
a. Khi càng lên cao thì tỉ lệ lượng khí oxi càng giảm ?
b. Phản ứng cháy của các chất trong bình chứa oxi lại mãnh liệt hơn trong không khí ?
c. Vì sao nhiều bệnh nhân bị khó thở và các thợ lặn làm việc lâu dưới nước… đều phải thở bằng khí oxi nén trong bình đặc biệt ?
Bài giải:
a) Khi càng lên cao tỉ lệ lượng khí oxi trong không khí càng giảm là vì khí oxi năng hơn không khí (nặng hơn rất nhiều lần các khí khác như nitơ, heli, hiđro,…).
b) Phản ứng cháy của các chất trong bình chứa oxi mãnh liệt hơn trong không khí là vì khi cháy trong khí oxi, bề mặt tiếp xúc của chất cháy với oxi lớn hơn nhiều lần trong không khí. Trong khi cháy trong không khí, thể tích oxi chỉ chiếm 1/5 lần, phần còn lại là hầu hết nitơ và các khí khác, bề mặt tiếp xúc của chất cháy sẽ nhỏ hơn và một phần nhiệt sẽ bị tiêu hao do đốt nóng khí nitơ trong không khí.
c) Bệnh nhân khó thở và người thợ lặn làm việc lâu dưới nước phải thở bằng khí oxi vì khi oxi cần cho sự hô hấp để oxi hóa chất dinh dưỡng trong cơ thể người sinh ra năng lượng để duy trì sự sống của cơ thể.
3. Hướng dẫn giải bài tập Sách bài tập Hóa học 8 bài 25:
Bài 25.1 trang 34
Trong các công thức hoá học sau, công thức nào là công thức của oxit: SO2, CH4O, CO2, NaOH, P2O5, Fe3O4, Al2O3 ?
Bài giải:
Công thức của oxit: SO2, CO2, P2O5, Fe3O4, Al2O3.
Bài 25.2 trang 35
Trong các phản ứng hóa học sau, phản ứng nào là phản ứng hóa hợp ?
a) 4Al + 3O2 2Al2O3
b) Fe + H2O FeO + H2 ↑
c) CaCO3 CaO + CO2
d) SO3 + H2O H2SO4
e) CaO + CO2 CaCO3
f) CaO + H2O Ca(OH)2
Bài giải:
Các phản ứng là phản ứng hóa hợp :
a) 4Al + 3O2 2Al2O3
d) SO3 + H2O H2SO4
e) CaO + CO2 CaCO3
f) CaO + H2O Ca(OH)2
Bài 25.3 trang 35
a) Củi, than cháy được trong không khí. Nhà em có củi, than xếp trong hộc bếp, xung quanh có không khí. Tại sao củi, than đó lại không cháy ?
b) Củi, than đang cháy em muốn dập tắt thì phải làm thế nào ?
Bài giải:
a) Củi, than cháy được trong không khí phải có mồi của ngọn lửa để nâng lên nhiệt độ cháy còn than củi xếp trong hộc bếp xung quanh có không khí nhưng không cháy vì ở nhiệt độ thấp hơn nhiệt độ cháy.
b) Củi, than đang cháy em muốn dập tắt thì phải để chúng không tiếp xúc với oxi của không khí, do đó vẩy nước hay phủ cát lên bề mặt vật cháy để cho vật không tiếp xúc với không khí và hạ nhiệt độ xuống dưới nhiệt độ cháy.
Bài 25.4 trang 35
Cho các oxit: CO2, SO2, P2O5, Al2O3, Fe3O4.
a) Chúng được tạo thành từ các đơn chất nào ?
b) Viết phương trình hoá học của phản ứng và nêu điều kiện phản ứng (nếu có) điều chế các oxit trên.
Bài giải:
a) Các oxit được tạo thành từ các đơn chất :
CO2: được tạo ra từ đơn chất cacbon và oxi.
SO2: được tạo ra từ đơn chất lưu huỳnh và oxi.
P2O5: được tạo ra từ đơn chất photpho và oxi.
Al2O3: được tạo ra từ đơn chất nhôm và oxi.
Fe3O4: được tạo ra từ đơn chất sắt và oxi.
b) Phương trình hoá học của phản ứng điều chế các oxit:
C + O2 CO2
S + O2 SO2
4P + 5O2 2P2O5
4Al + 3O2 2Al2O3
3Fe + 2O2 Fe3O4
Bài 25.5 trang 35
Phải trộn hỗn hợp C2H2 và O2 với tỉ lệ nào về thể tích thì phản ứng cháy sẽ tạo ra nhiệt độ cao nhất ? Phản ứng này được ứng dụng để làm gì ?
Bài giải:
Phương trình phản ứng đốt cháy khí C2H2 :
2C2H2 + 5O2 4CO2 + 2H2O
2 mol → 5 mol
Để có phản ứng cháy xảy ra ở nhiệt độ cao nhất thì tỉ lệ thể tích:
VC2H2 : VO2 = 2 : 5 = 1 : 2,5
Ứng dụng của phản ứng này dùng trong đèn xì oxi – axetilen để hàn và cắt kim loại.
Bài 25.6 trang 35
a) Biết tỉ lệ khối lượng của hai nguyên tố nhôm và oxi trong nhôm oxit bằng 4,5 : 4. Công thức hoá học của nhôm oxit là
A. AlO. B. AlO2. C. Al2O3. D. Al3O4.
b) Oxit của một nguyên tố có hoá trị II chứa 20% oxi (về khối lượng). Công thức hoá học của oxit đó là
A. CuO. B. FeO. C. CaO. D. ZnO.
Bài giải:
a) Công thức của oxit là AlxOy
Tỉ số khối lượng:
Ta có tỉ lệ:
Vậy công thức hóa học của nhôm oxit là Al2O3.
⇒ Chọn đáp án C.
b) Công thức hóa học của oxit cần tìm là MO
Ta có trong 100 g MO có 20 g oxi
Vậy M + 16 g MO có 16 g oxi
Ta có tỉ lệ:
Vậy M là kim loại Cu, công thức hóa học của oxit là CuO.
⇒ Chọn đáp án A.
Bài 25.7 trang 35
Một oxit của lưu huỳnh trong đó oxi chiếm 60% về khối lượng. Tìm công thức phân tử của oxit đó.
Bài giải:
Gọi công thức hóa học của oxit là: SxOy
Ta có, phân tử khối của SxOy là: 32x + 16y (đvC)
Theo đề bài oxi chiếm 60% về khối lượng nên ta có:
Tỷ lệ:
Vậy công thức hóa học của oxit là SO3.
Đây là nội dung tóm tắt và giải bài tập Chương 4 bài 25: Sự oxi hóa – Phản ứng hóa hợp – Ứng dụng của oxi trong chương trình hóa học lớp 8 mà các bạn có thể tham khảo. Mời các bạn cùng tham khảo các bài viết tương tự trong chuyên mục : Hóa học lớp 8